L’Agence fédérale des médicaments et des produits de santé (AFMPS) a annoncé la mise en ligne d’une nouvelle rubrique recensant les dispositifs médicaux (DM) et dispositifs médicaux de diagnostic in vitro (IVD) dont l’indisponibilité pourrait entraîner un préjudice grave ou un risque de préjudice grave pour les patients ou la santé publique.
Cette initiative découle de l’entrée en vigueur début janvier 2025 d'un nouveau réglement européen. Ces textes imposent aux autorités compétentes de signaler les dispositifs absents temporairement (interruption) ou définitivement (cessation) du marché national.
La liste, accessible sur le site de l’AFMPS, est alimentée sur base des informations transmises par les fabricants et les acteurs de la chaîne d’approvisionnement, sous leur propre responsabilité. Elle s’adresse en priorité aux professionnels de la santé, aux patients ainsi qu’aux distributeurs et autres intervenants du secteur qui souhaitent être informés de l’évolution du marché.
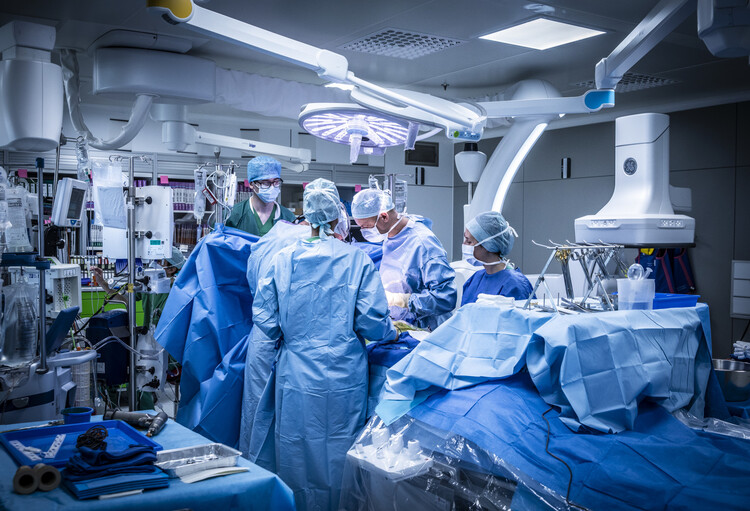
Actuellement une vingtaine de disposititifs médicaux sont renseignés indisponibles , comme par exemple, les tubes trachéaux Portex® destinés à l'intubation orale et/ou nasale pour la gestion des voies respiratoires ou encore des accessoires stériles à usage unique facilitant la circulation extracorporelle et l’oxygénation lors de procédures chirurgicales, avec transfert de fluides et connexion à d'autres dispositifs médicaux.
Les dispositifs concernés sont ceux mis sur le marché de l’Union européenne et dont l’indisponibilité sur le marché belge pourrait avoir des conséquences graves. L’AFMPS précise que la liste sera régulièrement mise à jour en fonction des notifications reçues.
> Découvrir la liste des indisponibilités des dispositifs médicaux